Результаты исследования и обсуждение
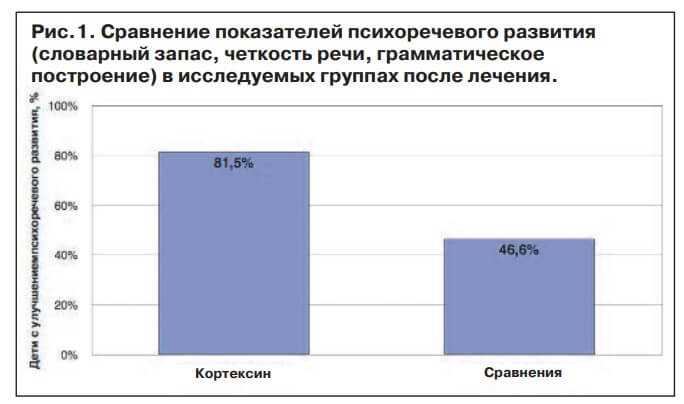
В результате лечения имело место улучшение показателей психоречевого развития как у детей 1-й, так и 2-й подгруппы. Отмечались коррекция звукопроизношения, автоматизация звуков, расширился словарный запас, улучшилась лексика, грамматика, компенсировались психоневрологические нарушения. На фоне лечения Кортексином показатели психоречевого развития улучшились у 39 детей из 2-й подгруппы, что составило 81,5% (в группе сравнения аналогичный показатель составил 46,6% — 21 ребенок) (рис.1).
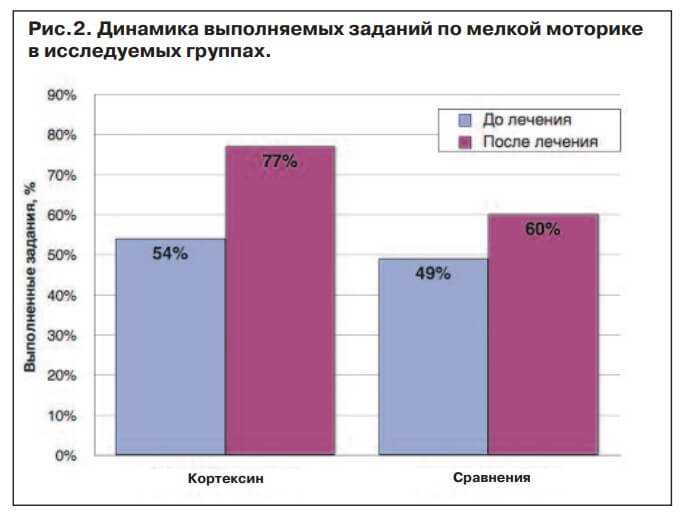
Помимо психоречевого развития, имела место положительная динамика при выполнении заданий по мелкой моторике. В группе детей, которые в составе комплексного лечения получали Кортексин, процент выполняемых заданий увеличился на 23%, а в группе сравнения — на 11% (рис.2).
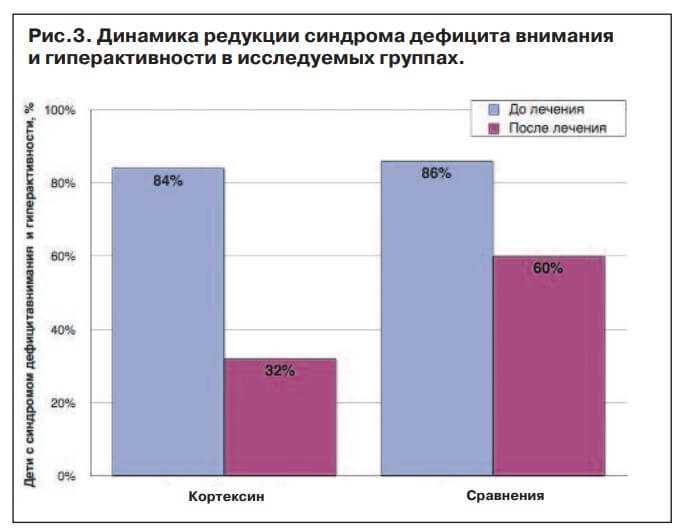
Редукция клинических признаков синдрома дефицита внимания и гиперактивности в группе детей, получавших Кортексин, так же проходила более быстрыми темпами (рис.3).
Кроме анализа психоречевого и моторного развития, нами были оценены ультразвуковые критерии. Основные паттерны, выявленные за весь период наблюдения: мозаичная асимметрия индекса резистентности (resistanceindex — RI), внутрибассейновая асимметрия, диффузное повышение RI, снижение линейных скоростей кровотока (ЛСК) в каротидном бассейне, снижение ЛСК в вертебробазилярном бассейне, цереброваскулярная реактивность (ЦВР) — вазодилататорный и вазоконстрикторный тесты, скорость венозного оттока по базальным венам, ширина третьего желудочка, глубина залегания затылочных рогов боковых желудочков. Эти показатели в процессе лечения также претерпевали изменения(табл. 2).
Из полученных данных следует, что в течение 1 года статистически значимое (p<0,05) изменение частоты встречаемости тех или иных ультразвуковых паттернов отмечено как у детей 1-й, так и 2-й групп. При этом уменьшение доли пациентов с мозаичной и внутрибассейновой асимметрией индексов сопротивления, измененной ЦВР (отрицательный вазодилататорный тест), расширенным более 5 мм третьим желудочком, увеличением глубины залегания затылочных рогов боковых желудочков более 16мм происходило достоверно быстрее в группе, где применялся Кортексин (p<0,05). В ходе исследования было установлено, что динамика диффузного повышения RI, вазоконстрикторного теста, скоростных показателей кровотока в базальных венах не зависела от типа выбранного лечения, так как в обеих группах произошло достоверное снижение доли детей (p<0,05). Достоверно оценить динамику синдрома диффузного повышения RI между группами затруднительно из-за низкой частоты данного паттерна в обоих случаях (11%— 1-я группа; 14,6% —2-я группа).
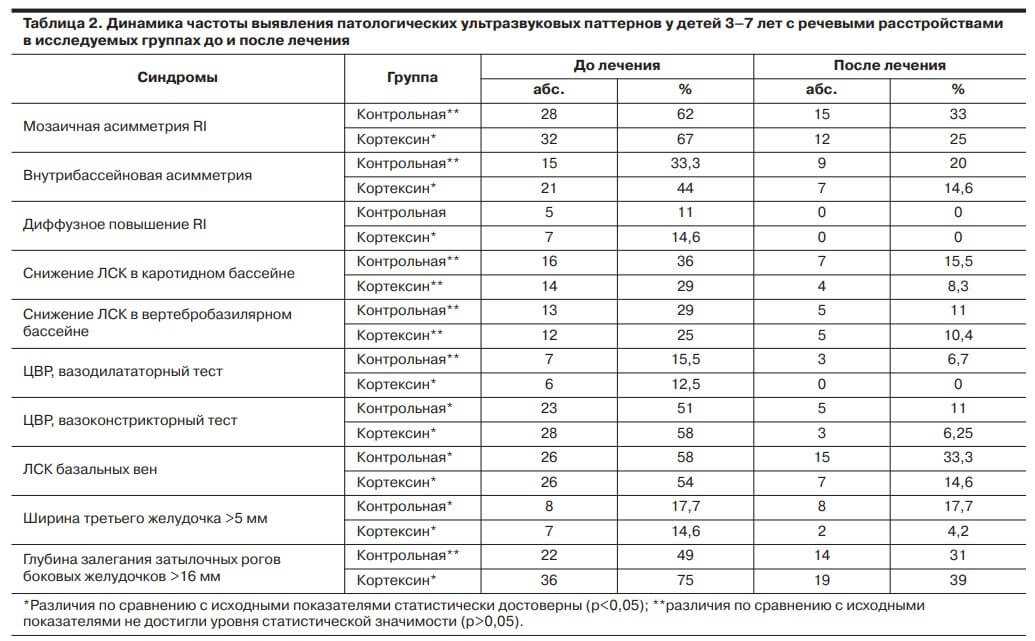
Статистически недостоверное изменение показателей (p>0,05)отмечается по синдромам снижения ЛСК в каротидном и вертебробазилярном бассейнах, что связано с исходно низкой частотой данных ультразвуковых нарушений в обеих группах, и динамика редукции частоты этих синдромов также одинакова.
Таким образом, характеризуя динамику неврологического и логопедического статуса у детей двух групп во время исследования, необходимо отметить, что пациенты, в чей план лечения входил Кортексин, показывали более стабильные результаты в восстановлении речевой функции (звукопроизношение, лексика, грамматика), компенсации неврологической симптоматики. Полученные клинические данные коррелируют с положительной динамикой ультразвуковых синдромов. Оценивая ультразвуковые критерии, выявили, что введение в схему лечения препарата Кортексин обеспечивает улучшение гемодинамики и у большего количества пациентов в виде нормализации сосудистого сопротивления и ЦВР, восстановления внутрибассейновой симметрии кровотока. Значимого влияния на ЛСК по результатам исследования Кортексин не оказывал. Это подтверждает, что в основе терапевтического эффекта препарата Кортексин при лечении речевых расстройств лежит его способность непосредственно влиять на метаболизм нервных клеток, ускоряя морфофункциональное созревание структур головного мозга и формирование связей между разными отделами центральной нервной системы.
Антиоксиданты
В основе положительного эффекта лежит двойственная способность препаратов этого вида.
С одной стороны, возможность нейтрализации свободных радикалов. Если говорить понятнее, под термином понимаются ионы различных веществ. При контакте с сосудистой стенкой, клетками головного мозга и прочими структурами, они вступают в реакцию окисления, что вызывает разрушение и в конечном итоге приводит к множеству заболеваний.
Способность нейтрализации свободных радикалов помогает восстановлению работоспособности клеток и сохранению их функциональной активности. Также предотвращает раковые процессы в организме, пусть и косвенным образом.
С другой стороны, антиоксиданты повышают степень переработки кислорода. Иными словами, КПД газообмена резко растет. При прежнем количестве O2 в организме, его оказывается достаточно для обеспечения основных процессов.
На этом механизме и строится вся работа антиоксидантов. В чистом виде подобных медикаментов крайне мало. Обычно они обладают несколькими фармакологическими возможностями.
Список препаратов нейропротекторов антиоксидантного типа:
Глицин — классический медикамент, относится к ноотропным средствам. Но за счет способностей нейромедиатора и ускорения утилизации кислорода, борьбы со свободными ионами в организме его можно причислить и к антиоксидантам.
Используется в клинической практике наиболее широко. В основном за счет высокой эффективности и низкой стоимости. Однако же, высока вероятность аллергических реакций. При приеме нужно внимательно следить за самочувствием.
Мексидол. Средство со сравнительно узкой сферой применения. В основном его назначаются в рамках коррекции энцефалопатии и прочих дисциркуляторных нарушений. Возможно применение для профилактики ишемического инсульта, других подобных процессов.
Мексидол назначается врачами в качестве средства для комплексного лечения, но не для монотерапии (одного единственного).
Глутаминовая кислота. Схожа по клиническим возможностям с Глицином, но имеет большую сферу применения.

Эмоксипин. Назначается в качестве средства для лечения последствий инфаркта, инсульта, также патологий глазного происхождения и профиля. Например, глаукомы, диабетической ретинопатии. Спектр случаев, когда возможно применение довольно узок.

Антиоксиданты обладают смешанными качествами, что делает их пригодными для назначения во множестве ситуаций. Не считая группы исключений.
Основные терапевтические эффекты Кортексина
Благодаря тому, что средство влияет на все мозговые процессы, оно отличается большим количеством эффектов, имеющих важное терапевтическое значение
- Ноотропный – Кортексин при ЗРР стимулирует все высшие функции ГМ. Отмечается стимуляция памяти и способности к обучению, повышение стрессоустойчивости.
- Нейропротекция. Препарат защищает нейроны ГМ от нейротоксических элементов, способствующих их разрушению. Он эффективен в отношении эндо- и экзогенных токсических агентов.
- Антиоксидантный. Кортексин уколы при ЗРР препятствуют окислительному стрессу, и увеличивают способность нейронов выживать и работать в условиях недостатка кислорода.
- Метаболический. Средство повышает скорость обменных процессов в ГМ, стимулирует процессы регенерации, улучшает тонус вегетативной и симпатической нервных систем, а также работу коры ГМ.
Оценка результатов
Активность клеток головного мозга отражается на дисплее. Это позволяет врачу распечатать данные и расшифровать показатели более точно. Полученные данные значительно облегчают и ускоряют постановку диагноза пациенту.
Не пытайтесь разобраться в результатах энцефалограммы самостоятельно. У каждого человека скорость импульсов отличается, особенно это распространяется на детей.
При постановке диагноза врач-невропатолог будет также учитывать данные анамнеза ребенка, результаты дополнительных исследований.
Оценка колебаний
На основании данных обследования на энцефалограмме отображаются ритмы работы головного мозга:
- Основной ритм или альфа ритм регистрируется в затылочных отделах.
- Бета колебания максимально определяются в лобной области.
- Тета и дельта ритмы максимально регистрируются во время сна ребенка.
Плюсы и минусы нейролептиков
В последние годы в медицине большой упор делается на исследование биологической природы психических заболеваний. В частности, серьезные прорывы были сделаны в направлении изучения процессов, происходящих в головном мозге, при появлении или развитии различных симптомов. Это стало толчком к стремительному развитию психофармакологии, в частности, сегодня при лечении как взрослых пациентов, так и детей, применяются новые препараты, более эффективные и безопасные.
При лечении речевых и поведенческих нарушений у детей чаще применяются атипичные нейролептики — медикаменты второго поколения, характеризующиеся более мягким воздействием, более безопасные.
Но нужно понимать, что к сегодняшнему дню доказательства безопасности нейролептиков последнего поколения существуют лишь в отношении краткосрочного применения. Большая часть исследований продолжается до одного года, так что о долгосрочных перспективах лечения говорить нет смысла. Ситуация усугубляется еще и тем, что детям антипсихотики часто назначают по медицинским показаниям, которых нет в официальных документах к препаратам, то есть, речь идет об их избыточном употреблении.
Шкала BSID-II
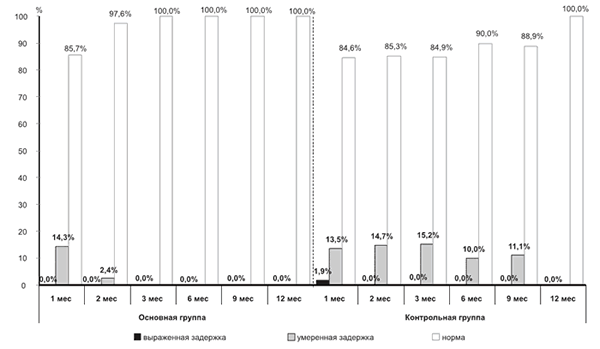
Сравнительный анализ результатов тестирования детей сравниваемых групп по BSID-II показал, что в СВ 1 мес средние индексы как психического, так и моторного развития в группах сравнения были сопоставимы. Однако показатель психического развития соответствовал диапазону «выраженная задержка развития» у детей контрольной группы достоверно чаще, чем в основной группе; Χ2 (df=1)=4,7; p=0,03 (рис. 2). К СВ 3 мес индекс моторного развития был достоверно выше у детей основной группы (98,3±7,05) по сравнению с контрольной (93,42±7,74); t(df=67)=2,74; р=0,008. При этом оценки всех детей основной группы по шкале психического развития соответствовали диапазону «оптимальное развитие». В то же время в контрольной группе оценки 15,15% детей соответствовали диапазону «умеренная задержка развития»; Χ2(df=1)=5,88; p=0,015. При сравнении индексов моторного развития в СВ 3 мес имела место тенденция к более высоким его значениям у детей основной группы по сравнению с контрольной (97,75±6,66 и 94,64±9,54 соответственно), однако различия не достигали степени статистической значимости. В то же время при анализе распределения оценок по диапазонам имели место достоверные различия: оценки 21,21% детей контрольной группы соответствовали «умеренной задержке развития», в то время как в основной группе оценки всех детей соответствовали «оптимальному развитию»; ??(df=1)=8,5; p=0,004. В дальнейшем индексы как психического, так и моторного развития всех детей основной группы соответствовали диапазону «оптимальное развитие» на протяжении всего периода наблюдения (до СВ 12 мес). В интервалах от 3 до 6 мес и от 9 до 12 мес отмечалось достоверное увеличение индекса моторного развития — t(df=31)=—2,6; р=0,014 и t(df=22)=—3,85; р=0,001 соответственно. При этом средние индексы психического и моторного развития детей контрольной группы на протяжении всего периода наблюдения оставались ниже, чем в основной группе (рис. 3). Оцениваемые индексы у всех детей стали соответствовать диапазону «оптимальное развитие» только к СВ 12 мес.
 |
|
Рис. 2. По оси ординат — доля детей (%), имевших значение индекса психического развития по BSID-II, соответствующее диапазонам «выраженная задержка развития», «умеренная задержка развития» и «норма». |
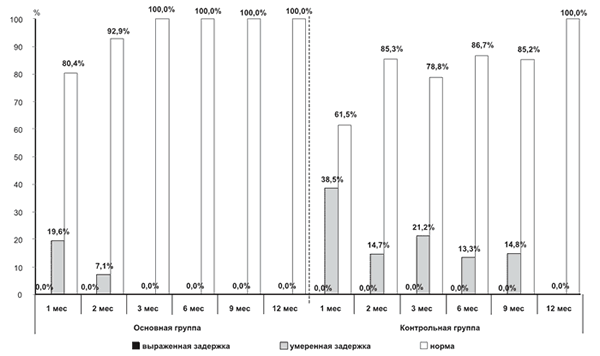 |
|
Рис. 3. По оси ординат — доля детей (%), имевших значение индекса моторного развития по BSDI-II, соответствующее диапазонам «выраженнаязадержка развития», «умеренная задержка развития» и «норма». |
Таким образом, у детей, получавших цитофлавин в остром периоде перинатального гипоксически-ишемического поражения, отмечалось более успешное и быстрое формирование нормативных показателей нервнопсихического развития на 1-м году жизни.
Когда назначают инъекционные препараты
Существующие нормы развития речевого навыка позволяют говорить о существенных задержках лишь после 3-х лет. До этого возраста возможно наблюдение логопеда и невролога с немедикаментозной коррекцией. Для этого родители выполняют ряд упражнений вместе с ребёнком в кабинете у специалиста или дома.
Если к трём годам речь не наладилась, может быть выставлен диагноз «специфическое расстройство речевого развития». Оно подразумевает отставание ребёнка от возрастных критериев по умению разговаривать, но отмечается сохранность уровня интеллекта, слуха и есть комфортные условия для обучения. В анамнезе исключены нейроинфекции и травмы мозга и костей черепа. Цикличности в течении болезни не отмечается.
Но сама по себе задержка развития речи не может быть показанием к немедленному началу инъекционной терапии. Выбор методики подразумевает наблюдение за пациентом не менее полугода и попытки коррекции щадящими способами. Если они не приносят положительного результата, подключаются препараты в виде уколов.
Как помочь здоровому развитию ребенка?
Многие современные родители, которые хорошо понимают, что ММД – не особенность характера, а проблема, которую можно устранить или уменьшить, уделяют большое внимание правильному выбору безопасных и эффективных препаратов. Нейропептид «Семакс 0,1%» устраняет дисбаланс регуляторных систем в коре мозга, улучшает образование новых связей между нейронами
Препарат нормализует развитие коры полушарий мозга, регулирует работу его функциональных центров
Нейропептид «Семакс 0,1%» устраняет дисбаланс регуляторных систем в коре мозга, улучшает образование новых связей между нейронами . Препарат нормализует развитие коры полушарий мозга, регулирует работу его функциональных центров.
Научно доказано, что «Семакс 0,1%» является одним из наиболее эффективных препаратов для улучшения памяти у детей. Серьезный положительный эффект препарата в развитии нервной системы ребенка подтверждается тем, что его успешно применяют не только для лечения ММД, но и для развития детей с нарушением интеллекта.
Многочисленные исследования препарата «Семакс 0,1%» подтвердили его способность повышать концентрацию внимания, которая очень важна для занятий в школе, а также сопротивляемость стрессам, усидчивость и усвоение информации. При минимальных мозговых дисфункциях лечение с применением «Семакса 0,1%» способствует развитию речевых, коммуникативных и прочих навыков, важных для хорошей социальной адаптации и успехов в учебе.
Правила приема «Семакса 0,1%»
Прием 20 дней
По 2 капли в каждый носовой ход 2 раза в день последнее закапывание до 17:00
Курс 3 флакона 2-4 курса в год
- во флаконе содержится 60 капель
- закапывание производить строго на слизистую носа, не допуская протекания в носоглотку
Синдром «нехочухи»
Дети с ММД по уровню интеллекта и способностей не уступают сверстникам. Но дисбаланс в работе отдельных участков коры больших полушарий мозга приводит к задержке темпов развития важнейших функциональных систем мозга (речи, восприятия, внимания, памяти, двигательных навыков и других).
Нарушения в развитии ребенка могут проявляться:
- Проблемами с чтением (дислексией)
- Нарушением письма (дисграфией)
- Нарушениями речевых функций
- Проблемами со счетом (дискалькулией)
- Проблемами с двигательным развитием (отставание от возрастных норм)
- Синдромом дефицита внимания и гиперактивностью
Сочетание проявлений минимальных мозговых дисфункций между собой может быть очень разным. Но почти всегда результатом ММД является дезадаптация в коллективе, проблемы в учебе, возможны частые конфликты с родителями и учителями. Дети с трудом концентрируются на задании, допускают много ошибок при его выполнении, ведут себя непредсказуемо и импульсивно. И когда речь заходит об учебе или другом занятии, которое вызывает у ребенка трудности, родители сталкиваются с громкими капризами и заявлениями «Не хочу!». По данным статистики проявления ММД можно встретить не менее чем у 20% школьников.
Характер не исправишь?
Ученые выяснили, что такие нарушения в развитии ребенка часто имеют наследственный фактор. Поэтому многие родители списывают проблемы с поведением и возникшие трудности в учебе на характер ребенка («пошел характером в папу, маму, или деда…») и надеются, что все пройдет с возрастом. В результате ребенок не успевает приобрести важные для него знания и опыт в определенном возрасте, а это может плохо сказаться на его будущем (поступление в ВУЗ, выбор круга общения и так далее).
Нарушение памяти у детей и другие проявления ММД требуют помощи специалиста, а также применения препаратов для улучшения работы центральной нервной системы. Психолого-педагогические коррекционные занятия научат ребенка и родителей справляться с задачами, которые вызывают трудности, улучшат взаимопонимание. Но одних занятий чаще всего недостаточно, особенно, если речь идет о существенных нарушениях в развитии ребенка. Одной из причин развития ММД является снижение пластичности нейронов и медлительность в создании новых межнейронных связей в головном мозге. Поэтому центральной нервной системе ребенка требуется поддержка, чтобы обеспечить слаженную работу клеток мозга, устранить дисбаланс в работе отдельных участков коры больших полушарий.
Механизмы действия препарата
Препарат оказывает мощное стимулирующее воздействие на процессы, происходящие в центральной нервной системе. Он состоит из водорастворимых нейропептидов с малой молекулярной массой. Это обеспечивает их легкое проникновение в ткани головного мозга (ГМ). Основные механизмы действия отмечаются за счет:
- стимуляции нейротрофических элементов, нейронов и регуляторных пептидов;
- нормализации количества аминокислот, образующихся в ГМ;
- подавления судорожной активности ГМ;
- нормализации электрической активности мозга;
- торможении процессов формирования свободных радикалов в тканях ГМ.
Поскольку Кортексин при задержке речевого развития вводится только парентерально, он сразу проникает в кровь и ткани ГМ. Это обеспечивает быстрое развитие его лечебных эффектов.

Дозировка и способ введения Кортексина
Средство выпускается в виде стерильного порошка для самостоятельного приготовления раствора и его внутримышечного введения.
Какой растворитель лучше использовать решит врач, он же определит нужную дозировку. Как правило, Кортексин детям при ЗРР назначается следующим образом.
| Возраст | Растворитель | Место введения | Суточная доза |
| До года | Вода для инъекций/физиологический раствор | Передняя поверхность бедра | До 0,3 мг/кг массы тела |
| 1-3 года | Вода для инъекций/физиологический раствор | Передняя поверхность бедра или ягодица | 0,4-0,6 мг/кг |
| 3 -5 лет | Новокаин или вода для инъекций | Ягодичная мышца | 5-7 мг/ сутки |
| Старше 5 лет | Новокаин или вода для инъекций | Ягодичная мышца | 10 мг/сутки |
Ноотропные медикаменты
Эта группа лекарственных средств используется в качестве поддерживающей меры. В основном назначается короткими курсами, однако возможно длительное систематическое применение. Вопрос остается на усмотрение врача.
В основе фармакологического эффекта лежит несколько способностей:
- Ускорение синтеза специфических веществ, которые обеспечивают нормальную проводимость нервных волокон. Это главное качество подобных наименований.
- Стабилизация регенеративных свойств, увеличение интенсивности всех процессов заживления. В основном это требуется для пациентов после неотложных состояний вроде инсульта или гематомы, травмы.
- Восстановление нормального газообмена. Препараты ноотропного действия способствуют коррекции кислородного обеспечения нервных тканей. Учитывая, что головной мозг крайне требователен к концентрации O2, этот эффект наблюдается практически с первых приемов.
Помимо, косвенным образом ноотропы обеспечивают нормальную умственную активность и способны восстановить память, когнитивные способности в короткие сроки
Однако при применении и назначении вообще нужно проявить осторожность
Высокие дозировки вызывают побочные эффекты. Кроме того, стоит иметь в виду, что при наличии опухолей головного мозга любой локализации является абсолютным противопоказанием для использования ноотропов. Поскольку велика вероятность ускоренного роста неоплазии. В том числе доброкачественной, вплоть до типичной аденомы гипофиза. Это прямой путь к психическим и органическим нарушениям.
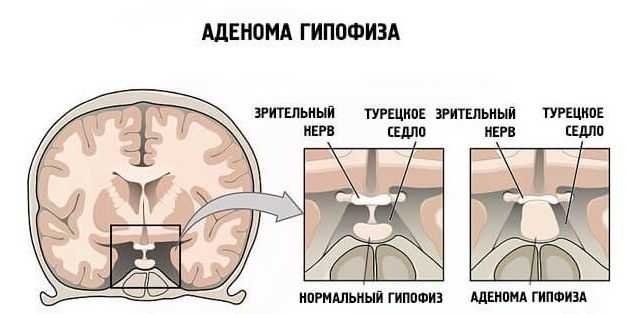
Наименований нейротропных препаратов для восстановления обменных процессов в головном мозге множество. Рассмотрим особенно популярные в медицинской среде.
Пирацетам
Едва ли не самые первый из медикаментов рассматриваемого типа. Применяется в широком перечне ситуаций, является своего рода универсальным наименованием. В основном назначается в качестве меры профилактики или терапии хронических ишемических процессов мозга.
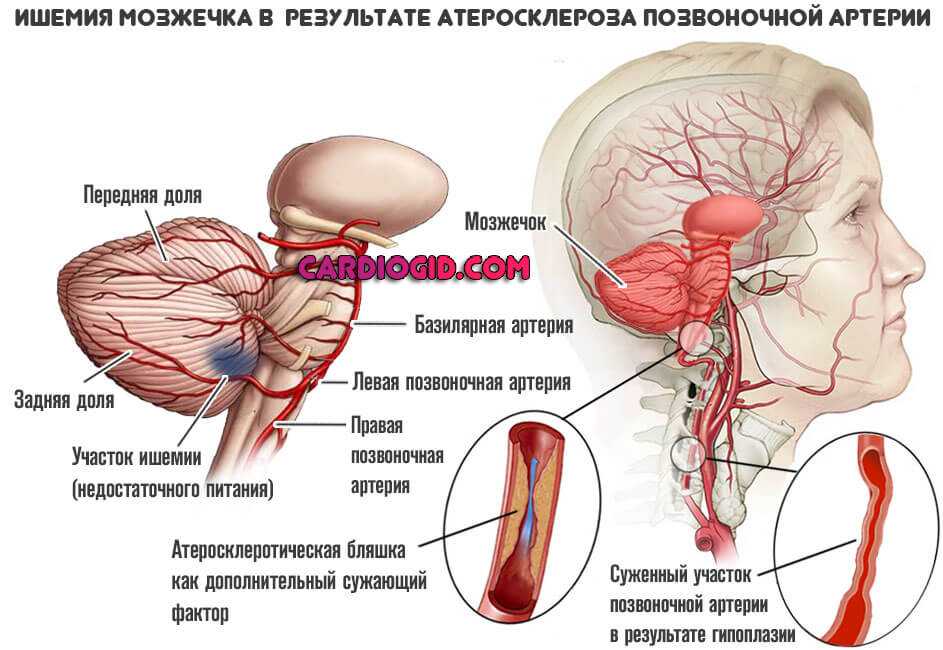
Требуется довольно длительный курс для коррекции когнитивных способностей, нарушений питания головного мозга.
Имеет минимум побочных эффектов, потому несмотря на давность существования все еще сохраняет позиции в условных рейтингах врачей-неврологов.

Цераксон
Имеет узкую сферу использования, восстанавливает мембраны нервных клеток и предотвращает их дальнейшую гибель. Среди показаний выделяют перенесенные травмы любого характера, также ишемические и геморрагические инсульты.
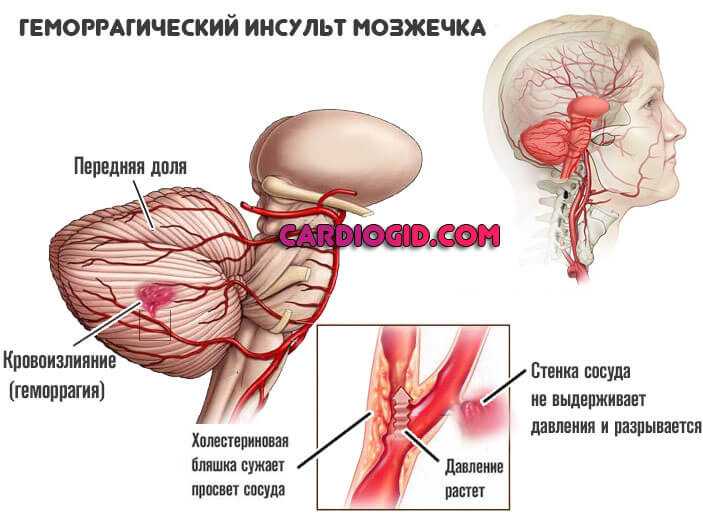
Имеет смысл применять подобный препарат в рамках всего реабилитационного периода.
Отказ происходит постепенно, до тех пор, пока состояние не вернется в норму. В дальнейшем в качестве вторичной профилактики назначаются другие медикаменты.
Церебролизин
Примерно равен по интенсивности нейропротекторного эффекта Пирацетаму. Создается на основе препарата головного мозга свиней, выпускается в форме раствора для инъекций. Имеет природное, естественное происхождение. Потому противопоказаний минимум, как и вероятности побочных эффектов.
Тем не менее, по своему усмотрению принимать лекарство нельзя. Последствия непредсказуемы.
Семакс
Является смешанным нейропептидом, обеспечивает не только ускорение нейрометаболизма, но и восстановление адекватного кровотока. Относится к синтетическим, универсальным средствам, применяется по усмотрению специалистов.

Есть и другие названия, однако они назначаются куда реже. Вопрос выбора необходимого медикамента зависит от конкретного клинического случая.
Подробный обзор ноотропов читайте здесь.
Когда показана детям ЭЭГ?
Методика позволяет определить состояние нервной системы малыша. Она основана на передаче электрических импульсов нейронами, создающими биоэлектрическую активность головного мозга. Что это такое – ЭЭГ для детей? Электроэнцелограф отображает полученную информацию в виде кривых линий в разные периоды активности. Если врач направил ребенка на обследование, не стоит отказываться от проведения исследования. Оно безболезненно и в то же время достаточно информативно для выявления патологий головного мозга различного характера.
Врач назначает ребенку ЭЭГ в следующих случаях:
- при периодически повторяющейся потере сознания;
- если ребенок выпадает из реальности;
- после черепно-мозговой травмы средней степени тяжести;
- при эпилептической клинике;
- стойких нарушениях сна;
- при подозрении на онкологические процессы;
- для контроля процесса реабилитации после перенесенной нейрохирургической операции;
- в случае врожденной патологии (напр. гидроцефалия);
- при нарушениях мозгового кровообращения;
- при нарушениях в неврологическом статусе (детский церебральный паралич, другие двигательные нарушения);
- при расстройствах аутистического спектра;
- задержке развития, как в психической, так и в физической сфере.
Электроэнцефалография показывает локализацию очагов эпилептиформной активности, степень и динамику заболевания, эффективность подобранной терапии. Поэтому область ее применения очень широка.
Иногда врач направляет ребенка на ЭЭГ даже при отсутствии определенных соматических патологий. Показаниями к ее проведению являются отклонения в поведении, развитие, несоответствующее возрасту, слабая память и отсутствие концентрации, гиперактивность. В школьном возрасте при чрезмерно быстрой утомляемости также может быть назначена электроэнцефалограмма головного мозга для детей.
Метод широко используется с целью диагностики эпилепсии.
Показатели ЭЭГ при различных патологических состояниях в педиатрии
ЭЭГ предоставляет возможность диагностировать различные заболевания, такие как эпилепсия, аутизм и детский церебральный паралич. Она также помогает оценить функцию мозга при коматозных состояниях, синдроме гиперактивности, слабоумии и ишемии мозговой ткани. Изменения ритма на ЭЭГ могут быть связаны с наличием тиков у детей. Например, регистрируются изменения альфа-ритма, нарушение ритмики волн, вспышки тета-волн низкочастотной амплитуды, высокоамплитудные бета-волны и единичные неспецифические острые волны. Также может быть отмечено повышение или снижение основного ритма. У детей с аутизмом на ЭЭГ обнаруживается доминирующий тета-ритм, который указывает на трудности адаптации в обществе. Во время лечения выраженность тета-волн снижается, а альфа-ритм нарастает. Иногда также может наблюдаться усиление бета-волн. Пациенты с эпилепсией младенчества на ЭЭГ могут показывать усиление электрической активности в виде острых ассиметричных волн, пиков и комплексов пик-волна. Лучше проводить электроэнцефалографию во время сна, так как в дневное время изменения на ЭЭГ могут быть незаметны, особенно при ночной форме эпилепсии. Если сон недоступен, можно использовать пробы стимуляции, такие как двигательная, гипервентиляционная или зрительная. У пациентов с синдромом гиперактивности на ЭЭГ может быть обнаружена медленноволновая активность альфа-ритма при гипервентиляционной пробе. Без стимуляции изменений на ЭЭГ практически не наблюдается, за исключением снижения связи между полушариями. Во время комы на ЭЭГ часто обнаруживается бета-ритм в виде веретен сна, что свидетельствует о жизнедеятельности мозга. При слабой мозговой активности могут быть обнаружены специфические паттерны. При наступлении смерти мозга на ЭЭГ выявляется изолиния. ЭЭГ при коме необходима для определения состояния пациента и дальнейшего ведения его лечения. Также по ЭЭГ можно изучать реакцию мозга на введение лекарственных препаратов. У пациентов с синдромом Дауна и дистрофией мозговой ткани электрическая активность будет снижена. Амплитуда альфа-ритма будет низкой, а ответ головного мозга на стимуляцию будет слабым. При детском церебральном параличе также могут быть обнаружены эпилептиформные признаки на ЭЭГ, так как этот синдром также связан с повреждением мозга.
Полезные советы
СОВЕТ №1
При диагностике различных заболеваний у детей с помощью ЭЭГ, важно обратить внимание на наличие эпилептиформных активностей. Они могут свидетельствовать о наличии эпилепсии или других неврологических расстройств. При обнаружении таких активностей необходимо обратиться к специалисту для дальнейшей диагностики и лечения
При обнаружении таких активностей необходимо обратиться к специалисту для дальнейшей диагностики и лечения.
СОВЕТ №2
Оценка фоновой активности ЭЭГ также является важным критерием при диагностике заболеваний у детей. Нормальная фоновая активность характеризуется ритмичностью и симметрией. Отклонения от нормы могут указывать на наличие патологических процессов в мозге. При обнаружении аномалий необходимо проконсультироваться с врачом для дальнейшей диагностики и лечения.
Выводы
В проведенном исследовании показана возможность эффективного амбулаторного лечения пациентов с нарушением речевой функции. При этом получены следующие результаты. 1. Применение Кортексина способствует регрессу неврологической симптоматики, ускоряет темпы речевого развития и улучшает качество речи. 2. У детей, получавших в составе комплексного лечения Кортексин, быстрее компенсировались сосудистые дистонии, нормализовались показатели ЦВР. Таким образом, применение Кортексина оправдано, эффективно и может рекомендовано для лечения и комплексной реабилитации детей с речевыми нарушениями в амбулаторных условиях.























